【杭州佳业康复医院】经鼻导管高流量氧疗,开展脑梗、心肺康复
发布时间:2023-01-20 11:32:00 点击次数:一、什么是鼻导管高流量吸氧呢?
临床上通常使用低流量系统(如鼻导管或面罩)或高流量系统(如文丘里面罩或非重复呼吸面罩)来给患者输送氧气。这些传统给氧系统并不能提供可靠的吸入氧分数(fraction of inspired oxygen, FiO2),并且因为吸入气体未进行充分的加温和湿化,患者通常难以长时间耐受。尽管经鼻导管高流量氧疗(high flows through nasal cannulae, HFNC)通常应用于婴幼儿,但随着能可靠地输送加温加湿氧气的HFNC新系统的研发,该装置在成人中的应用也越来越多。

二、临床上怎么样获益呢?
使用经鼻导管高流量氧疗输氧的获益机制如下图。主要的终末器官效应是改善舒适度和氧合指数。

机制包括
鼻导管小且易弯曲
HFNC鼻导管一般柔软且易弯曲。因此,一些研究报道,与传统的经鼻导管低流量给氧或面罩高流量给氧相比,使用HFNC的舒适度有所改善。
分泌物的加温和湿化
将要吸入的高流量氧气(通常>40L/min)加温至核心温度比通过低流量氧气加温更为有效。因此,HFNC对吸入氧气的加温加湿效果优于传统的高流量给氧系统,例如文丘里面罩或非重复呼吸面罩(流量通常为10-15L/min),或低流量给氧系统(流量<10L/min)。加湿可增加黏膜的湿度,从而有利于分泌物清除,也可减少呼吸功,避免气道干燥和上皮损伤。
冲刷鼻咽部死腔
输送大量氧气可冲刷掉上呼吸道通气死腔,提高通气效率,并改善氧输送。因此,与其它氧气输送系统相比,HFNC冲刷性能的改进可增加有效通气量,即参与肺泡气体交换的每分钟通气量。
持续气道正压效应
持续气道正压(continuous positive airway pressure, CPAP)效应——成人的多项研究表明,HFNC会增加鼻咽部的气道压力,并在呼气末时达到峰值,即“呼气末气道正压(positive end-expiratory pressure, PEEP)效应”。这种“PEEP效应”可能消除潜在的内源性PEEP,减少呼吸功,改善肺泡填充性病变[例如充血性心力衰竭或急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)]患者的氧合。患者的鼻咽部压力随着流量的增加而增加(即剂量效应)[10]。口腔闭合时应用CPAP效应最为明显。一般情况下,在口腔闭合时,流量每提升10L/min可产生大约0.7cmH2O的气道压力,而张口时则为0.35cmH2O。因此,其CPAP效应充其量为轻至中度。
高流量
使用HFNC时,高流量可尽可能避开夹杂室内空气,从而使氧气输送更为精确,这种效应与传统的输氧系统相比尤为明显。处于呼吸窘迫的患者会出现很高的吸气流量,甚至超过标准吸氧设备的流量,因而会夹入室内空气,导致实际FiO2低于设置值。HFNC的流量通常超过患者吸气流量,仅夹杂极少量的室内空气,因此输送的FiO2更可靠。但是,类似于传统输氧系统,张口呼吸或运动时喘气会在某种程度上减弱此优势。也有研究表明高流量能通过提高潮气量和降低呼吸频率来改善患者的呼吸模式。
减少吸气用功
增加流量可减少吸气用功,二者呈线性关系。通常以较低流量就能实现二氧化碳清除。
三、大致的使用和设置
HFNC氧疗的应用越来越广泛。目前尚无针对其实际应用的既定推荐建议;因此下述建议仅代表我们自己的实践经验。尽管HFNC可用于无监护的病房,但我们认为最好用于有监护的环境,例如ICU、中等强度监护病房或急诊室。对此,我们的倾向性建议理由基于:需要HFNC的患者存在发生严重呼吸衰竭或机械通气的高风险,在这种情况下,通常需要进行严密监测。然而,一旦患者的病情改善,对氧的需求逐渐降低(例如流量为50L/min,FiO2为60%),可降低HFNC的监测需求。
氧气从供氧源输出,在被加温和湿化以后,经过宽口径鼻导管输送给患者;该鼻导管通常是一种比低流量系统的吸氧管更软、更易弯曲的塑料管。鼻导管紧贴鼻孔,并用头带固定。
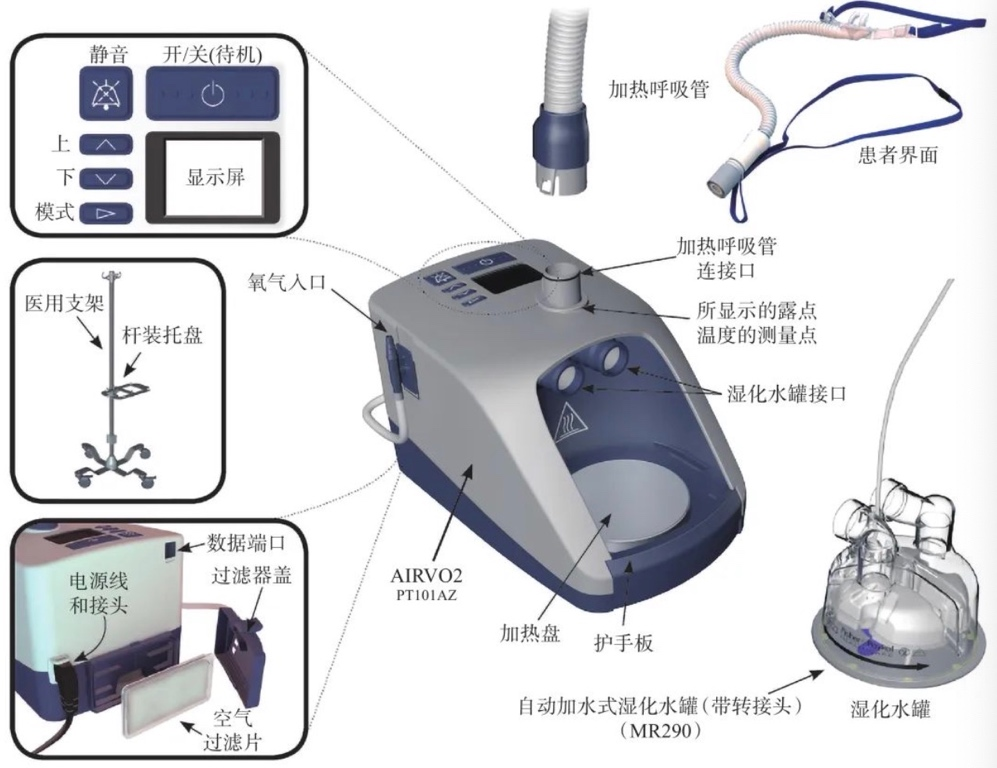
只需要设置两个参数:
① 流量
② 给氧浓度(FiO2)
我们倾向于先设置流量,通常为20-35L/min(范围为5-60L/min),然后再设置FiO2(范围为21%-100%)以达到所需的外周血氧饱和度。如果呼吸频率没有改善、氧合指数没有充分改善或呼吸仍费力,随后可按每次5-10L/min增加流量。增加流量和FiO2都可改善外周血氧饱和度;我们倾向于先把流量调至最大,以便使FiO2≤60%;但有时可能需要增加FiO2才能充分改善氧合。
HFNC通常耐受性良好,并且可以较长时间应用(例如数天)。一旦患者的流量≤20L/min且FiO2≤50%,可切换为传统的低流量鼻导管给氧系统。
